Dans le bilan , sauf exception, on obtient un cycle à 6 centres , à partir d'un diène (le plus simple étant le butadiène ) en conformation cis , et d'une autre liaison pi entre 2 atomes (la plus simple étant celle de l'éthylène) . Ce deuxième réactif est le diénophile. Un diène peut aussi jouer le rôle de diénophile (voir ci-dessous )
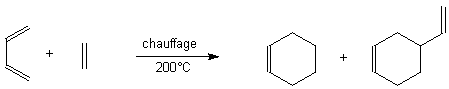
majoritaire
Le produit majoritaire est ici issu de la réaction du diène "butadiène" avec le diénophile "butadiène".
Le produit minoritaire s'est formé par réaction du diène "butadiène" avec le diénophile "éthylène" .
1- modèle de hückel : les orbitales frontière
Cette réaction est sous contrôle cinétique et s'interprète dans le cadre du modèle des orbitales frontières, selon Hückel.
Un schéma mécanistique dans ce modèle serait :
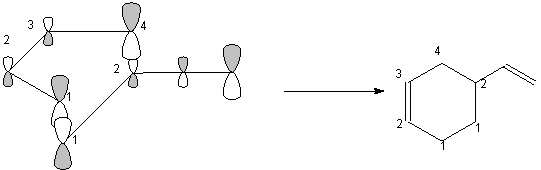 et
et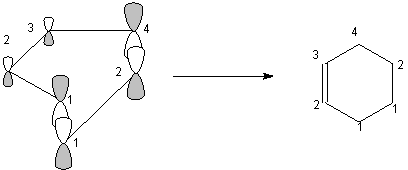
Cliquer ici pour voir une animation Flash de la réaction de Diels Alder ( bouton bleu )
La réaction ne peut se faire que si elle est permise par symétrie
La réaction est permise par symétrie si les coefficients des atomes (1,4) et ( 1',2' ) des réactants forment des paires de même symétrie de signe . Autrement dit, si 1 et 4 ont des coefficients de même signe, il faut alors que 1' et 2' aient des coefficients de même signe, quel que soit ce signe. Si 1 et 4 ont des coefficients de signe opposé, il faut alors que 1' et 2' aient des coefficients de signe opposé.
C'est l'intéraction entre la HO et la BV les plus proches en énergie des réactants qui permet de prévoir la réaction .
La réaction est d'autant plus rapide que la HO et la BV sont plus proches.
Un groupe donneur d'électrons sur le diène ou le diénophile augmente le niveau d'énergie des OF.
Groupes donneurs : -O-Me , -R, ...
Un groupe attracteur d'électrons sur le diène ou le diénophile diminue le niveau d'énergie des OF.
Groupes attracteurs : -C=O , C=N , ...
Conséquence :
C'est la HO du porteur du donneur et la BV du porteur de l'attracteur qui seront les plus proches, plus proches que dans le cas du système butadiène/éthylène, pris en réference. La réaction sera donc plus rapide.
Le porteur du donneur réagit donc comme un nucléphile, alors que le porteur de l'attracteur réagit comme un électrophile.
Si les deux portent un groupe donneur (ou un attracteur ) ...seule l'étude précise des énergies relatives des OF permet de conclure .
Règle d'Alder :Un groupe donneur (respectivement attracteur ) sur le diène et un groupe attracteur sur le diénophile ( respectivement donneur ) accélèrent la réaction de Diels Alder.
Ceci justifie du résultat de la réaction citée en introduction : le dénophile butadiène est un éthylène aui porte un groupe donneur, alors que le diène ne porte rien...cela accélère quand même la réaction / butadiène , éthylène
2-Régiosélectivité
La réaction est sous contrôle orbitalaire :
La HO et la BV les plus proches en énergie ayant été identifiées , c'est l'intéraction entre les atomes de plus gros coefficient dans chacune des OF en intéraction qui oriente ( régiosélectivité ) la réaction .
Ces plus gros coefficients sont donnés par les résultats de Hückel , pris en valeur absolue.
Ils peuvent PARFOIS être trouvé grâce au modèle de Lewis ( on rappelle que ces modèles sont différents mais peuvent être complémentaires) , à condition que l'on soit dans le cas de la règle d'Alder, c'est à dire un donneur sur un réactant et un attracteur sur l'autre :
Si le réactant porte un groupe donneur : il intervient par sa HO
Quel que soit le groupe donneur présent , remplacez-le par -O-Me : O porte un doublet libre , donneur d'électons : il vous permet d'écrire des formes mésomères, avec création de charges . Ecrivez la plus longue chaîne de résonance possible : Le porteur de la charge - est aussi le porteur du plus gros coefficient de la HO .
Si l'autre réactant porte un groupe attracteur : il intervient par sa BV
Quel que soit le groupe donneur présent , remplacez-le par -CH=O : Le doublet pi de C=O peut se rabattre sur O, et créer un chaîne de délocalisation: écrivez la forme mésomère avec la plus longue chaîne de délocalisation : Le porteur de la charge + est aussi le porteur du plus gros coefficient de la BV .
Exemple :
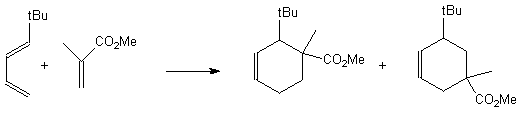
MAJORITAIRE minoritaire
Ce résultat est prévisible aussi bien par l'étude des résultats de Hückel (1/ recherche des OF, 2/ recherche du plus gros coefficient dans chaque OF ) que par l'étude des formes mésomères .
3-Stéréospécificité
Cliquer ici pour voir une animation Flash de la réaction de Diels Alder ( bouton rouge)
Lors de l'attaque du diène par le diénophile , on distingnue les positions endo (notés d) et exo (notés x ) des groupes portés par le diénophile :
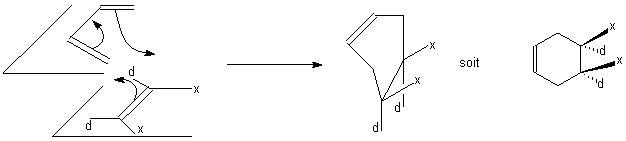
Les deux groupes endo seront donc forcément du même côté du plan moyen du cycle ( et même chose pour les groupes exo ) : la réaction est donc stéréospécifique, par rapport au diénophile : un alcène Z et un alcène E ne donneront pas le même produit final.
Exemple :
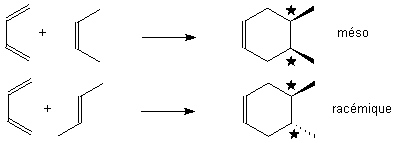
Mais la réaction est aussi stéréospécifique par rapport au diène :
Si le diène porte des groupes sur ses carbones 1 et 4 , ceux-ci présenteront une position liée aux groupes endo et exo :
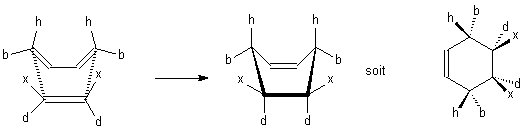 Les groupes
notés h (pour haut) et et les groupes exo seront donc du même côté du
plan moyen du cycle , et de même pour les groupes notés b
(pour bas) et les groupes endo .
Les groupes
notés h (pour haut) et et les groupes exo seront donc du même côté du
plan moyen du cycle , et de même pour les groupes notés b
(pour bas) et les groupes endo .De plus, certains groupes ont une préférence pour une position, endo ou exo :
Lors de l'intéraction entre les orbitales frontières, si le diènophile porte un groupe attracteur, le coefficient de l'atome lié au doublet pi en réaction permet une intéraction secondaire stabilisante avec un carbone "interne" du système pi du diène : ce groupe attracteur se dispose donc en ENDO par rapport au diène.
Inversement , c'est une intéraction secondaire déstabilisante qui aurait lieu avec un groupe donneur du diénophile . Un groupe donneur se dispose en EXO par rapport au diène,.
En résumé un donneur se place en EXO, un attracteur en ENDO .
Conséquence : On peut donner les exemples suivants :
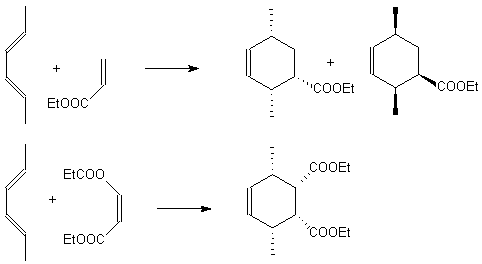
Comme l'hexa2,4 diène, est de configuration E,E, les méthyl sont en position "bas" , et les groupes COOEt , attracteurs se placent en endo.
Conclusion :
La réaction de Diels Alder est donc une méthode de créaction de liaison C-C, de création de cycles, régiosélective et stéréospécifique, sous contrôle orbitalaire.